Alexander Swarbrick 博士が最近バイオアーカイブに発表した論文「An experimental comparison of Digital Spatial Profiling and Visium spatial transcriptomics technologies for cancer research」は、DSPとVisiumプラットフォームの比較分析について深く掘り下げています。 どちらの技術も、乳がん組織の空間的プロファイリングにおいて立派な知見を示し、それぞれ異なる応用分野で輝きを放っています。
腫瘍の複雑なランドスケープ:先進的空間オミックスツールの必要性
腫瘍は単なるがん細胞の集積ではありません。 それどころか、さまざまな細胞サブタイプが入り組んだ生態系を形成しています。 腫瘍内のがん細胞の空間的組織は、治療に対する腫瘍の進行や応答に影響を及ぼす、がんの分子的な複雑さを知る治療濃度域を提供します。 多重免疫蛍光法のような従来の方法では、深部しか探ることができません。 空間オミックス技術の新たな領域は、このギャップを埋める可能性があります。 その中でも、NanoString GeoMx® Digital Spatial Profiling (DSP)vと10x Genomics Visium プラットフォームは、研究者が腫瘍の不均一性の包括的理解を得ることができるため、注目を集めています。
掘り下げの比較:DSPとVisiumプラットフォーム
実験の仕組み
DSP と Visium の厳密な比較のために、研究者たちは4つの原発性乳がん組織サンプルと2つの培養細胞株を用いた複雑な実験の仕組みを考案しました(図1)。 このアプローチにより、腫瘍の多様な細胞間相互作用特性の詳細な調査が可能になりました。
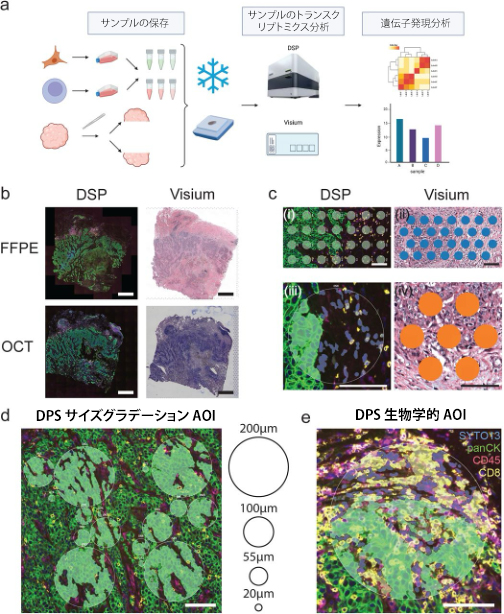
(a)サンプル保存と実験ワークフローの概略図。培養Jurkat細胞とSKBR3細胞を6種類の比率で混合し、OCTまたは FFPE サンプルとして保存した。組織サンプルは中央でスライスし、得られた2片をそれぞれOCTまたはFFPEサンプルとして保存した。DSPおよび Visium アッセイには、可能な限り近い切片を使用した。 このイラストは BioRender.com で作成された。 (b)組織形態の画像例。サンプル4806の FFPE およびOCT切片をDSPまたはVisiumアッセイ用に処理した。 FFPEサンプルとOCTサンプルの間、および DSP と Visium アッセイに使用した切片の間で、全体的に形態が一致していることに注意されたい。 スケールバー=1mm。 (c)直接比較に使用した DSP AOI と Visium スポットの例。 (i) 腫瘍-間質界面にわたる Visium 模倣 AOI の例。 (ii) DSP と Visium の直接比較に使用した腫瘍-間質界面を横切る Visium スポットの例。 (iii) 分割された比較DSP AOI の例。 各AOIは免疫蛍光シグナルに従って汎サイトケラチン陽性と汎サイトケラチン陰性に区分された。 (iv) 分割された比較 DSP AOI が収集されたマッチング領域に位置する Visium スポットの例。 スケールバー=100μm。 (d)DSPプラットフォームの分割性能をテストするためのサイズグラデーションと生物学的DSP AOIの例。 スケールバー=100μm
Key Observations
- 遺伝子発現相関: 制御されたセルアレイサンプルにおいて、2つのプラットフォーム間で高い相関が観察されました。 しかし、乳がん組織の複雑な性質から、遺伝子検出能力に微妙な違いがあることが判明しました。
- 組織の深堀分析: 両プラットフォームとも組織分析において素晴らしい深さを示しましたが、OCT処理サンプルの Visium は、 FFPE と比較して遺伝子検出においてわずかに時間的な遅れが生じました。 この組織調製の微妙な違いが結果に大きく影響します。
プラットホームの強さに注目
- Visium by 10x Genomics: その偏りのないアプローチにより、Visium は組織全体の包括的なランドスケープを提供します。 この鳥瞰図によって、研究者は空間的不均質性を詳細に解明することができます。 Visiumは、初期の探索的研究段階に優れています。広範な組織領域にわたる全トランスクリプトームを提供します。
- NanoString GeoMx DSP: 一方、DSP は精度に優れています。 複雑な分子プロファイリングに焦点を当て、特定の関心領域を深く掘り下げるその独自の能力は、仮説に基づいた研究にとってかけがえのないツールとなります。
DSP で特定領域を探る
DSP プラットフォームの能力は、粒度の細かい領域にズームインしたときにさらに発揮されます。 この深堀りによって、CD8 T 細胞のような密接に関連した細胞種とその周囲の細胞との複雑な相互作用が明らかになりました(図2)。 しかし、このような緊密な細胞間相互作用の中でトランスクリプトミクスプロファイルの純度を確保することは、依然として難題です。
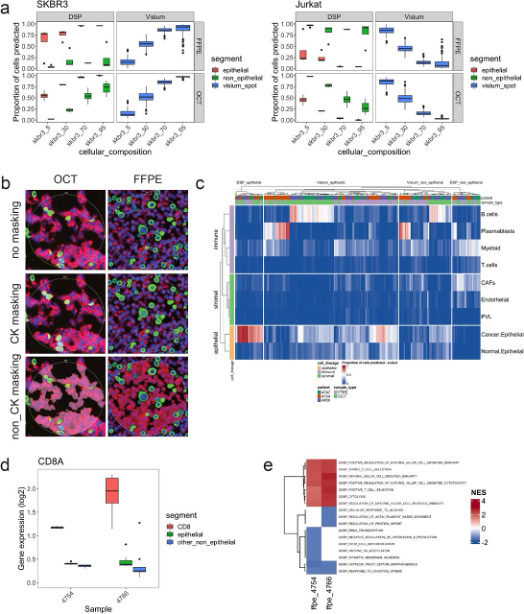
(a)細胞アレイサンプルのセグメント化された DSP AOI およびVisiumスポットにおけるSKBR3および Jurkat 細胞の予測割合。 (b)セルアレイサンプル上のセグメント化された DSP AOI の例。 すべての細胞を SYTO13 で核染色した。Jurkat 細胞は抗 CD45 抗体(赤)、SKBR3 細胞は汎サイトケラチン抗体(緑)でそれぞれ標識した。 上皮または非上皮の DSP AOI は、蛍光シグナルに基づいて順次サンプリングされた。 (c)組織サンプル中のセグメント化された DSP AOI および Visium スポットにおける、がんおよび TME 細胞タイプの予測割合。 (d)DSP データにおける CD8 セグメントと非 CD8 セグメントにおける CD8A の正規化発現。 (e)DSP プラットフォームにより CD8 セグメントと隣接する非 CD8TME セグメントとの間で同定された、有意に調節不全のある GOBP パスウェイの上位5つの NES。 有意性のしきい値はq < 0.25とした。
結論
空間トランスクリプトミクスの世界は万能ではありません。 DSP も Visium もそれなりに強力ですが、その選択は目の前の具体的な研究課題に帰結します。 この比較分析は、研究者が空間トランスクリプトミクスの可能性をフルに活用できるよう、情報に基づいた意思決定への道を開きます。




